Resumen
La luz se utiliza para aplicaciones de lo más diversas, dependiendo de su energía, es decir, de la región del espectro electromagnético a la que corresponde. A medida que conocemos más sobre sus propiedades, y que desarrollamos tecnologías para controlarla, aparecen nuevas aplicaciones.
Aquí se presenta una aplicación de la luz no muy difundida: las pinzas ópticas (también llamadas “trampas láser”). Si bien no es una técnica nueva, no cuenta con una amplia divulgación debido a que no tiene aplicaciones en la vida cotidiana. La técnica permite manipular objetos muy pequeños y determinar fuerzas muy débiles. Los sistemas biológicos se organizan justamente en esa escala de distancias, mediante interacciones en el orden de las fuerzas que la técnica permite determinar, por lo que la metodología permite aprender sobre los principios que rigen los procesos biológicos.
Palabras clave
Pinzas ópticas, motores moleculares, trampa láser, manipulación celular.
La luz ha sido, desde los comienzos de la especie humana, algo a lo que venerar y de lo que sacar provecho. Fuimos conscientes de que sin ella no hay vida, aun antes de conocer el proceso de fotosíntesis, y aun antes de saber detalles acerca de nosotros mismos. Por ejemplo, sin saber que la activación de la vitamina D depende de la luz y que, si no se activa, el calcio no se adsorbe correctamente, llevando a un esqueleto débil. Sin conocer que el ciclo luz-oscuridad diario regula nuestro reloj interno, el que a su vez regula los ciclos de actividad del organismo a través de los niveles de melatonina. Sin entender que las alteraciones de este ciclo llevan a alteraciones de nuestro estado de ánimo, al punto de que la luminoterapia (exponer al paciente a luz artificial) sea hoy un tratamiento antidepresivo muy extendido en los países nórdicos.
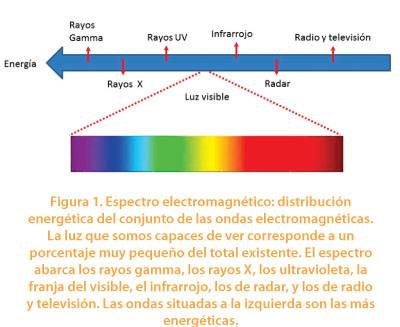
En los albores de nuestra especie, solamente éramos conscientes de la región del espectro electromagnético correspondiente a la luz visible (figura 1) y su utilidad era, principalmente, alumbrar y dar calor. Hoy sabemos que, además de la zona que somos capaces de percibir por medio de la visión, hay otras radiaciones electromagnéticas. Sabemos que algunas nos hacen daño aunque no las percibamos (o las percibamos débilmente) a través del tacto o de la vista, como la luz UV que provoca ceguera si nos exponemos por tiempos excesivos a la nieve sin lentes con un filtro adecuado, o la luz microondas, que usamos para calentar los alimentos, pero que nos haría daño si nos expusiéramos a ella.
A medida que aprendimos sobre la radiación electromagnética en las diferentes regiones del espectro, hemos ampliado su gama de aplicaciones. Ya hablamos de la utilidad de la región de las microondas, todos sabemos cuán útiles son los rayos X cuando nos quebramos un hueso, y no nos extraña que nos acerquen una lámpara de luz UV en la boca para acelerar la polimerización cuando vamos al dentista. Las ondas de baja frecuencia (de radar, radio y televisión) no necesitan ser presentadas, y con esto completamos una serie de ejemplos que ya forman parte de nuestra vida cotidiana.
En este texto hablaremos de otra utilidad de la luz, no muy reciente, pero de no tanta difusión debido a que sus usos están restringidos a experimentos de laboratorio en escalas muy pequeñas. Me refiero a las pinzas ópticas (o trampas láser). Fueron creadas en 1986 por Arthur Ashkin, aunque los principios básicos de su existencia ya habían sido expuestos mucho antes. En su teoría electromagnética, James Clerk Maxwell (1831-1879) propuso que la luz está constituida por ondas electromagnéticas que ejercen presión al propagarse. Posteriormente, Albert Einstein (1879-1955) y Max Planck (1858-1947) modelaron la luz como si estuviera formada por un flujo de partículas (fotones) capaces de ejercer presión al incidir sobre la materia.
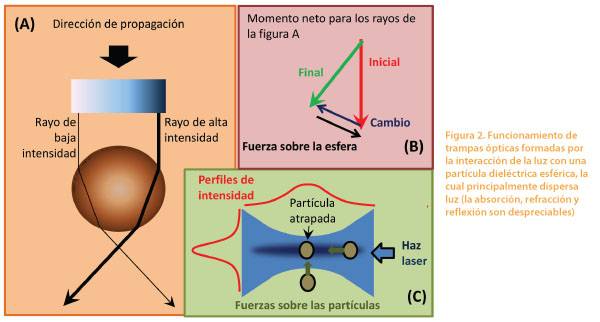 No voy a entrar aquí en detalles sobre la teoría detrás de esta técnica, simplemente diré que consiste en atrapar un objeto, y eventualmente moverlo, con luz. La trampa se encuentra en la región de mayor intensidad, como se muestra en la figura 2c. El lector interesado puede ver una brevísima descripción en la figura 2, o más detalle en el link indicado al final del texto y las referencias que allí se proveen. No voy a entrar aquí en detalles sobre la teoría detrás de esta técnica, simplemente diré que consiste en atrapar un objeto, y eventualmente moverlo, con luz. La trampa se encuentra en la región de mayor intensidad, como se muestra en la figura 2c. El lector interesado puede ver una brevísima descripción en la figura 2, o más detalle en el link indicado al final del texto y las referencias que allí se proveen.
Una vez convencidos de que la luz es capaz de ejercer presión, vale preguntarse por qué no nos aplastamos bajo el sol de verano (a veces sentimos esa sensación, pero eso es otro cuento, más relacionado con la desesperada necesidad de nuestros cuerpos de disipar calor para mantenerse a 37 ºC, que con el choque de fotones). Además, surge otra pregunta: si el efecto se predijo a mediados-finales del 1800, ¿por qué recién fue utilizado a finales del 1900?
La respuesta a ambas preguntas tiene que ver con cuál es el valor de presión que es capaz de ejercer un haz de luz si, por ejemplo, utilizamos un haz de 100 watts de potencia, será capaz de ejercer una fuerza máxima de 0,000001 N. Si esa fuerza se aplica sobre una superficie pequeña, pero aun de tamaños directamente visibles (digamos de 1 por 1 mm), se generará una presión de 0,00001 atmósferas. Este valor es totalmente despreciable en comparación con la presión atmosférica que soportamos continuamente (que es de alrededor de una atmósfera). Sin embargo, si la misma fuerza se aplica sobre una región mucho más pequeña (por ejemplo, sobre una célula) será capaz de generar presiones del orden de las diez atmosferas, lo cual sería similar a estar nueve metros por debajo del agua.
Mientras más pequeño y liviano sea el objeto, y mientras más intenso sea el haz de luz, mayor será el efecto provocado. Para poder iluminar con un haz intenso una superficie pequeña, fue necesario esperar al advenimiento de los láseres y es por ello que se tardó aproximadamente un siglo en utilizar lo que Maxwell, Einstein y Planck habían predicho.
La trampa se genera gracias a la “fuerza de gradiente”, la cual puede explicarse utilizando rayos ópticos, considerando una esfera de mayor tamaño que la longitud de onda de la radiación (A). La refracción de un haz de luz cuya intensidad varíe en el plano transversal genera un cambio de momento que debe ser balanceado por un cambio de momento en la esfera, lo cual produce la fuerza de gradiente (B). Por tanto, un haz de mayor intensidad en el centro atraparía la partícula en esa región de máxima intensidad. Para lograr atrapar a la partícula también en el eje de propagación, es necesario generar un gradiente de intensidad en este eje, haciendo converger el haz en un punto en el espacio (C). Con esta geometría se logra una trampa estable en la que cualquier movimiento arbitrario desde su centro genera una fuerza restaurativa. Para partículas de tamaño similar o menor a la longitud de onda, la aproximación de rayos ópticos no es válida y se utilizan otros modelos.
Hoy por hoy es posible generar un haz enfocado en una región de diámetro mucho menor al milímetro con una potencia de diez watts o mayor, lo que lleva a que sea posible mover objetos pequeños, o bien, mantenerlos quietos en un punto en el espacio, mediante la luz de una manera muy precisa. ¿Y para qué sirve esto? Más allá de haber sido un gran avance poder demostrar experimentalmente la validez de los modelos propuestos para describir el comportamiento de la luz, la técnica de pinzas ópticas permite manipular una única molécula con precisión y fuerzas comparables a las que existen en sistemas biológicos: es posible, mediante esta técnica, interrumpir o imitar procesos biológicos y así comprender los mecanismos y los principios que los rigen. Para estos usos, las pinzas suelen formarse utilizando luz visible o infrarroja, ya que son de baja energía y por tanto, no dañan la muestra. De las dos, se prefiere la luz infrarroja, ya que no interfiere en la observación.
Veamos un ejemplo. Los llamados “motores moleculares” son máquinas formadas por pocas moléculas, capaces de realizar trabajo a expensas de otro tipo de energía. Los motores moleculares que han sido más estudiados son las “kinesinas”, las cuales transportan cargas a lo largo de la célula, moviéndose sobre una especie de riel llamado “microtúbulo”. Este transporte se realiza a costa de energía química acumulada en el organismo (a través de la hidrólisis de ATP). Muy a grueso modo, las kinesinas constan de dos “pies” que “caminan” sobre los microtúbulos transportando la carga, como se muestra en la figura 3a. Mucho de lo que hoy se conoce sobre estas máquinas altamente eficientes se ha logrado entender mediante experimentos que emplearon pinzas ópticas, como el que se muestra en la figura 3b.
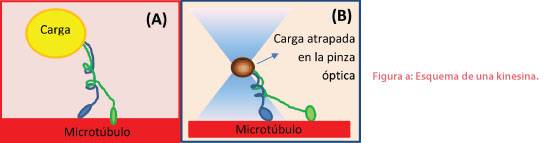
En 3a se muestra un esquema de la estructura propuesta para la kinesina, mientras que en 3b podemos ver un experimento típico que emplea pinzas ópticas. La carga es atrapada por la pinza, lo que permite medir la fuerza que realiza la kinesina al desplazarse por el microtúbulo. Simultáneamente, se determina la distancia que la carga es capaz de atravesar utilizando una cantidad conocida de energía química.
Estos y otros motores se han estudiado mediante trampas ópticas combinadas con otras técnicas. También se ha estudiado el plegado y estiramiento de moléculas como el ADN, el ARN y proteínas. Además, su uso permite manipular el interior celular sin provocar daño, ya que la pinza está hecha con luz. Asimismo, es posible mover una célula en particular dentro de un cultivo, y aplicar fuerzas locales a la membrana celular. En resumen, mucho se ha hecho en el área de la biología celular y de la biofísica utilizando pinzas ópticas, pero queda aún mucho más por hacer, ya que hoy por hoy, a pesar de los grandes avances que se han realizado, es muy poco lo que sabemos sobre cómo nuestro cuerpo trabaja para que podamos ver, oír, respirar, caminar… vivir.
Nota de la autora: Puede obtenerse más información en el siguiente link y en la bibliografía allí indicada: “Pinzas ópticas y su aplicación en biología” en Bitácora Digital, revista de la Facultad de Ciencias Químicas, Universidad Nacional de Córdoba. Vol. 1, Nº 2, año 2013. http://revistas.unc.edu.ar/index.php/Bitacora/article/view/5577 |




